Multiple Sklerose: Eine Krankheit der „falschen“ Darmbakterien?
Multiple Sklerose wird häufiger
Allein in Deutschland gibt es rund 200.000 Menschen, die an Multipler Sklerose (MS) erkrankt sind. Damit stellt die MS die zweithäufigste neurologische Erkrankung dar. Bei der MS handelt es sich um eine chronisch entzündliche, nicht ansteckende Erkrankung des zentralen Nervensystems, von der das gesamte Gehirn und Rückenmark betroffen sein können. An den Nervenzellen kommt es dabei zur sog. Demyelinisierung, einer irreversiblen Schädigung.
Die MS-Symptome können sehr unterschiedlich sein und von milden Verläufen bis zu schweren körperlichen und psychischen Einschränkungen reichen. Obwohl immer mehr Arzneimittel zur Symptomkontrolle und Reduktion der Schubrate verfügbar sind, gibt es bis heute keine kausale Therapie im Sinne einer Heilung.
Die Häufigkeit der MS nimmt seit Jahrzehnten zu, vor allem in den westlichen Industrienationen. Ein Teil dieses Anstiegs geht auf veränderte Diagnosekriterien und verbesserte Bildgebung zurück, wodurch eine MS heute besser diagnostiziert werden kann als früher. Allerdings deuten aktuelle Daten zunehmend darauf hin, dass unsere Lebensgewohnheiten einen maßgeblichen Einfluss auf die MS-Entstehung haben könnten.
Einen Überblick dazu, wie der Verlauf der Multiplen Sklerose durch Ernährung allgemein, bestimmte Diäten oder Mikronährstoffe beeinflusst werden kann, gibt es in dieser Podcast-Episode.
Umweltfaktoren als MS-Ursache?
Der genaue Mechanismus der MS-Entstehung ist trotz zahlreicher Hypothesen nach wie vor unklar. Vermutlich gibt es nicht eine einzige MS-Ursache, sondern bestimmte Umwelteinflüsse führen unter Beteiligung genetischer Faktoren zu einer Immunsystem-vermittelten Schädigung der Nervenzellen. Die MS ist definitiv keine Krankheit, die allein auf einer genetischen Veranlagung beruht.
Die Bedeutung dieser Umweltfaktoren wird auch durch folgende Beobachtung deutlich: Bei (genetisch praktisch identischen) eineiigen Zwillingen ist die Wahrscheinlichkeit, dass beide Zwillinge an MS erkranken, lediglich 30 % (Cree 2014). Aus Familienstudien weiß man schon lange, dass die individuelle Genetik nur ca. 30 % des MS-Risikos ausmacht, Umweltfaktoren und Lifestyle jedoch ca. 70 % (Farh et al. 2015). Wenn beispielsweise Kinder aus MS-Niedrigrisikoregionen (z. B. Afrika) in eine Hochrisikoregion (z. B. Europa) einwandern, haben sie anschließend ein vergleichbar hohes MS-Risiko wie die Einheimischen (Berg-Hansen et al. 2015). Diese Beobachtung deutet ebenfalls stark auf auslösende Umwelteinflüsse hin.
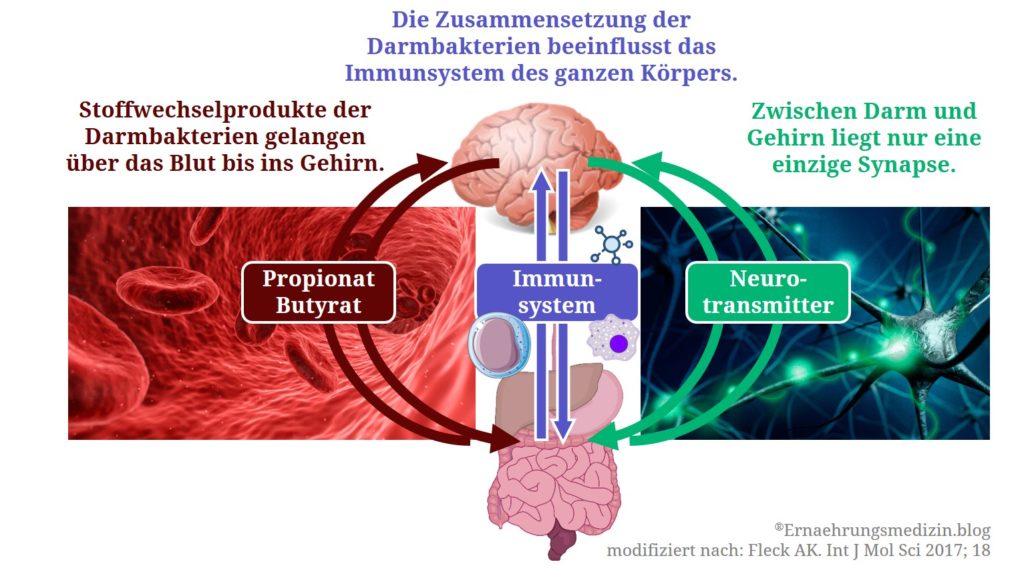
Neure Studien haben vermehrt Hinweise auf die wichtige Rolle von Darmbakterien für die MS-Entstehung geliefert (Chu et al. 2018). Welche Bakterienarten in unserem Darm leben, hängt maßgeblich von unseren Ernährungs- und Lebensgewohnheiten ab. Und seit Kurzem wissen wir: Die Darmbakterien sind keine passiven „Mitbewohner“, sondern über die sogenannten Darm-Gehirn-Achse beeinflussen sie unseren gesamten Stoffwechsel – auch im Gehirn (s. Abbildung, Colpitts et al. 2017). Jeder von uns trägt ungefähr 100 (!) mal so viele Darmbakterien in sich wie eigene, menschliche Körperzellen.
Da sich die Ernährungsweise in den vergangenen Jahrzehnten erheblich verändert hat und unsere Ernährungsgewohnheiten direkten Einfluss auf die individuelle Zusammensetzung der Darmbakterien besitzen, könnten auch Nahrungsbestandteile eine relevante Rolle in der MS-Entstehung spielen.
MS und Ernährungsfaktoren
Tatsächlich sind ernährungsmedizinische Aspekte sowohl in der Diskussion um die MS-Entstehung als auch im Rahmen der optimalen MS-Therapie relevant. So ist beispielsweise bekannt, dass Adipositas und Übergewicht bei MS-Betroffenen zwar ohne direkten Effekt auf den Krankheitsverlauf sind. Doch umgekehrt kann das Einhalten des Normalgewichts die Häufigkeit von Begleiterkrankungen reduzieren (Riccio & Rossano 2017, Jakimovski et al. 2019).
Da Gefäßerkrankungen und Krankheiten mit chronischen Entzündungsreaktionen wie z. B. Diabetes, Fettstoffwechselstörungen oder Bluthochdruck das Risiko für MS-assoziierte Gehbehinderungen erhöhen, trägt eine optimale Ernährungstherapie bei MS-Betroffenen indirekt zur Verbesserung der Prognose bei (Esposito et al. 2018).
Die Datenlage zur Sinnhaftigkeit der Vitamin-D-Supplementation ist für den Kontext der MS widersprüchlich. Klar ist jedoch, dass ein Vitamin-D-Mangel (< 30 ng/ml) die MS-Prognose verschlechtert (Riccio & Rossano 2017).
Hinweise auf Beteiligung der Darmbakterien
Aktuelle Studienergebnisse deuten nun darauf hin, dass die Darmbakterien einen maßgeblichen Effekt auf den MS-Verlauf haben könnten (Adamczyk-Sowa et al. 2017). In MS-Mausmodellen wurde gezeigt, dass Tiere unter keimarmen Bedingungen seltener erkranken als Tiere mit den üblichen Darmbakterien. Durch die experimentelle Beseitigung der gesamten Darmbakterien kann im MS-Mausmodell der Krankheitsausbruch sogar vollständig unterdrückt werden (Berer et al. 2011).
Zudem können in diesem Modell bestimmte probiotische Bakterien die Symptomatik verbessern (z. B. Bacteroides fragilis, Lactobazillen) oder verschlechtern (z. B. Lactobacillus farciminis) (Tankou et al. 2018). Erst vor Kurzem hatten Studienergebnisse für Aufsehen gesorgt, die einen relevanten Einfluss von Lactobazillen auf Bluthochdruck nahelegen (mehr dazu hier).
Vergleicht man die Darmbakterien-Zusammensetzung von Menschen mit MS und Gesunden, zeigen sich deutliche Unterschiede (Jangi et al. 2016): Insbesondere Acinetobacter– und Akkermansia-Arten finden sich bei MS-Patienten überdurchschnittlich häufig. Medikamentöse MS-Therapien können diese Akkermansia-Häufigkeit reduzieren, was möglicherweise ein Mechanismus ihrer Wirkung ist (Cantarel et al. 2015). Durch die Gabe eines bestimmten Lactobazillen-Mix (L. paracasei, L. plantarum) ist es in Studien möglich, die klinische MS-Symptomatik von Mäusen signifikant zu bessern (Tankou et al. 2018).
In einer wegweisenden Studie mit 34 eineiigen Zwillingspaaren, von denen jeweils nur ein Zwilling an MS erkrankt war, wurden die Stuhlproben auf Mäuse übertragen (Berer et al. 2017). Die Mäuse, die Stuhl von MS-Zwillingen erhalten hatten, erkrankten zu ca. 60 %; die Mäuse, die Stuhl der gesunden Zwillinge erhalten hatten, nur zu ca. 20 %. Dies deutet darauf hin, dass die Darmbakterien-Veränderungen bei MS-Patienten keine Folger der Erkrankung oder Therapie sind, sondern dass umgekehrt ein kausaler Zusammenhang existieren könnte (Libbey et al. 2018).
Kochsalz und Fettsäuren
In verschiedenen MS-Modellen zeigt sich außerdem ein Zusammenhang zwischen erhöhter Kochsalzzufuhr und einem schweren Krankheitsverlauf. Dies ist einigermaßen überraschend, da Kochsalz bisher vor allem als Risikofaktor bei Patienten mit Herzinsuffizienz (hier) oder Bluthochdruck (hier) diskutiert wird.
Als Mechanismus eines MS-verstärkenden Effekts von Kochsalz wird die Aktivierung salzabhängiger Signaltransduktion in einer bestimmten Art von Immunzellen (T-Helferzellen vom Th17-Typ) vermutet (Wilck et al. 2017). Th17-Zellen gelten als entscheidende Faktoren immunentzündlicher Erkrankungen (Kleinewietfeld et al. 2013).
Daneben könnte Kochsalz spezifische, entzündungsfördernde Effekte über die Darmbakterien vermitteln: So führt die erhöhte Salzzufuhr zur Abnahme von Lactobacillus-Spezies, und umgekehrt konnte die Supplementation mit (hochdosierten) Lactobazillen im Mausmodell die Aktivität der Th17-Zellen reduzieren und den Krankheitsverlauf positiv beeinflussen (Wilck et al. 2017).
In anschließenden Metabolom-Analysen wurde das von den Laktobazillen gebildete Tryptophan-Abbauprodukt Indol-3-Laktat als Auslöser dieser Effekte identifiziert (Wilck et al. 2017).
Im MS-Tiermodell bewirken mittel- und langkettige gesättigte Fettsäuren über die gesteigerte Aktivität der Th17-Zellen einen schwereren Krankheitsverlauf. Die Gabe kurzkettiger Fettsäuren dagegen (z. B. Propionsäure (Propionat) bewirkt einen milderen Krankheitsverlauf und reduziert die neuronalen Schäden (Melbye et al. 2019). Diese kurzkettigen Fettsäuren werden von den Darmbakterien aus faserreichen Lebensmitteln gebildet.
Daraus wurde die Hypothese abgeleitet, dass eine ballaststoffarme Ernährungsweise zu einer reduzieren Produktion kurzkettiger Fettsäuren im Dickdarm führt, wodurch ein bisher nicht definierter Mangelzustand entsteht, der wiederum die MS-Entstehung begünstigen könnte (Libbey et al. 2018).
Ausblick: Mikrobiom-basierte Therapieansätze
Nimmt man all diese Daten zusammen, ergeben sich verschiedene potenzielle Ansätze zur MS-Therapie (Zoledziewska 2019): Einerseits könnte man die Zusammensetzung der Darmbakterien von MS-Patienten gezielt verändern (z. B. durch Ernährungsumstellung oder Antibiotika).
Andererseits könnte man Bakterien, die den Krankheitsverlauf günstig beeinflussen, entweder in den Darm einbringen (z. B. in Form von Probiotika) oder sie im Wachstum fördern, indem die Patienten vermehrt faserreiche Lebensmittel zu sich nehmen (Präbiotika). Oder man könnte direkt die entscheidenden Stoffwechselprodukte der Darmbakterien supplementieren (z. B. Indol-3-Laktat oder Propionat).
All dies sind aktuell jedoch noch nichts weiter als experimentelle Ansätze, die in verschiedenen Studien erprobt werden. Die häufig angebotenen kommerziellen Tests zur Stuhluntersuchung von MS-Patienten sind jedoch sinnlos und sollten nicht empfohlen werden: Denn unabhängig davon, was die Stuhlanalyse für Hinweise auf Darmbakterien liefert – niemand weiß derzeit, wie die Ergebnisse zu interpretieren und welche Schlussfolgerungen daraus zu ziehen sind.
Gleiches gilt für die Anwendung von Probiotika-Präparaten. Es ist völlig unklar, welcher Bakterienstamm bei welchem MS-Patienten in welcher Dosierung welchen Effekt hat. Auch wenn ein Zusammenhang zwischen Darmbakterien und MS zunehmend plausibel ist – die Praxisrelevanz der Studiendaten ist zum jetzigen Zeitpunkt noch völlig ungeklärt.
Für Expert*innen: Die wissenschaftliche Datenlage zu Einfluss von Ernährungsfaktoren auf die Multiple Sklerose wird detailliert in einem Cochrane-Review (publiziert im Mai 2020) erläutert. Zur Anwendung von Vitamin D bei Multipler Sklerose gibt es ein separates Cochrane-Review aus dem Jahr 2017.
- Ernaehrungsmedizin.blog jetzt auf Instagram! - 18. Dezember 2023
- Neue Studie: Adipositas als Risikofaktor für Darmkrebs stark unterschätzt - 9. Juni 2023
- Ernährungsstrategie der Bundesregierung: Gerecht, gesund und nachhaltig soll sie sein - 21. Dezember 2022

Wieder einmal ein interessanter und hervorragend verfasster Artikel!
Danke für die gründliche Arbeit 🙂
Lieber Herr Smollich,
in diesem Zusammenhang eine Kasuistik aus meinem Krankenhaus . Ein Pat. mit einer MS (Gehstrecke 50 Meter) erhält wegen einer therapierefraktären Clostridieninfektion eine Stuhltransplantation. Neben der Clostridienelimination hat sich die Symptomatik der MS erheblich verbessert (Gehstrecke nahezu unbegrenzt).
Auch ich sehe da viel Potential
Hallo Herr Professor Doktor Kempa, Ich habe seit 14 Jahren MS und habe mich mit dem Thema beschäftigt und mich würde eine Stuhltransplantation sehr interessieren. Wie können wir in Kontakt für eine weitere Vorgehensweise kommen?
Lieber Martin,
ein sehr gut recherchierter und zusammengetragener Artikel. Unabhängig von der MS-Erkrankung – Beispiele mit identischen Zwillingen und der Einwanderung aus einem Niedrigrisikogebiet in ein Hochrisikogebiet gibt es einige. Sie unterstreichen die Macht der Ernährung und anderer Lebensstilfaktoren.
In Bezug auf kardiovaskuläre Gesundheit möchte ich deshalb beispielhaft folgende Studie erwähnen.
Kulshreshtha A, Goyal A, Veledar E, et al. (2014): Association between ideal cardiovascular health an carotid intimamedia thickness. a twin study. J Am Heart Assoc; 3(1):e000282
Liebe Grüße
Tim von vwissen.org
Vielen Dank für Deine positive Rückmeldung! Wenn man sich mit dem Thema beschäftigt sieht man ja, wie unglaublich groß die Nahrungseinflüsse auf die menschliche Gesundheit sind. Wir sollten das Beste daraus machen!
Sehr gut recherchierter Artikel. Danke.
Ich denke die Pflanzenzüchtung könnte auch eine bedeutende Rolle spielen.
Die Diskussion um den Weizen dürfte allgemein bekannt sein. Schon vor gut 10 Jahren hat mir ein Bekannter gesagt, dass er nur alte Apfelsorten verträgt. Er spritzt seine alten Sorten auch, aber moderne Sorten würde er vertragen. Vor einiger Zeit gab es dazu auch einen Beitrag bei „nano“.
Nun hat mir eine Dame erzählt, sie würde keine modernen Tomatensorten vertragen.
Und Off Topic:
Ich kann mir durchaus vorstellen, dass die überzüchteten Pflanzen auch einen Einfluss auf das Bienen-,Insektensterben,usw. haben.
lieber herr smollich,
toller artikel, ein bisschen geht mir die verbindung zu den mitochondrien ab. die erklärung von ms via reckeweg- schema ist schon sehr überzeugend. und da spielen eben die mitos vor allem in den phasen 4 und 5 eine entscheidende rolle.
herzliche grüße
dr. f.-j. schielein