Gewichtszunahme durch Psychopharmaka?
Psychopharmaka wie Antidepressiva und Schlafmittel gehören zu den am häufigsten eingenommenen Arzneimitteln in Deutschland. Leider besitzen diese Substanzen auch ein breites Spektrum an Nebenwirkungen, wodurch die Therapieadhärenz häufig reduziert bzw. eine Arzneimitteltherapie sogar unmöglich gemacht wird. Viele dieser Nebenwirkungen betreffen auch Körpergewicht, Appetit und Geschmacksinn.
Nebenwirkungen in Nutzen-Risiko-Abwägung einbeziehen
Da gerade bei der Anwendung von Antidepressiva die pharmakotherapeutischen Effektstärken oft begrenzt sind, sollte in der Nutzen-Risiko-Abwägung der Arzneimitteltherapie die Verträglichkeit, d. h. die Art und Ausprägung der Nebenwirkungen, besonders berücksichtigt werden. Die ernährungstherapeutische Antizipation oder Begleitung entsprechender Nebenwirkungen kann die Therapieadhärenz verbessern, und damit nicht nur die Nebenwirkungen abmildern, sondern auch den Erfolg der Arzneimitteltherapie insgesamt verbessern.
Häufige Nebenwirkungen von Psychopharmaka sind motorische Störungen, Reizweiterleitungsstörungen am Herzen (sog. QT-Zeit-Verlängerung), Blutbildungsstörungen und eben Effekte auf den Stoffwechsel (“metabolische Effekte”) (Benkert & Hippius 2017). Diese unerwünschten Stoffwechseleffekte umfassen v. a. Gewichtszunahme, Appetitsteigerung, erhöhte Harnsäurekonzentrationen, Fettstoffwechselstörungen sowie Störungen des Zuckerstoffwechsels (Crichton et al. 2016, Charles et al. 2016, Allison et al. 2009). Mit all diesen unerwünschten Wirkungen gehen eine teilweise erheblich erhöhte Krankheitslast und Sterblichkeit einher (Deng 2013).
Daneben gibt es aber sogar Psychopharmaka, die gerade wegen ihrer appetit- und gewichtsreduzierenden (Neben)Wirkungen beworben und angewendet werden; jüngstes Beispiel dafür ist die “Diätpille” Mysimba®.
Metabolische Effekte von Psychopharmaka sind sehr häufig
Anders als mitunter behauptet, erklärt die psychische Grunderkrankung die beobachteten metabolischen Veränderungen nicht ausreichend, sodass vieles auf einen zumindest teilweise kausalen Zusammenhang zwischen den eingesetzten Wirkstoffen und den unerwünschten metabolischen Effekten hindeutet (Padmavati et al. 2010; Sengupta et al. 2008). Parallel kann es auch durch die psychische Erkrankung an sich zu Veränderungen beispielsweise von Appetit und Körpergewicht kommen; gerade bei depressiven Erkrankungen ist dieser Zusammenhang mehr oder weniger ausgeprägt (Butnoriene et al. 2014, Zanoveli et al. 2016).
So konnte in einer prospektiven Kohortenstudie über zehn Jahre gezeigt werden, dass sich bei älteren Menschen das Risiko für einen Diabetes mellitus verdoppelt, nachdem eine Depression diagnostiziert wurde – und dieses erhöhte Diabetesrisiko war unabhängig von der antidepressiven Pharmakotherapie (Atlantis et al. 2010).
Zusätzlich muss aufgrund der Heterogenität der eingesetzten Wirkstoffe jede Substanz mit ihrer Studienlage einzeln betrachtet werden; eine Verallgemeinerung à la „alle Antidepressiva machen dick“ ist weder zutreffend noch hilfreich. Am ausgeprägtesten sind die Gewichtszunahmen bei der Anwendung von Antipsychotika; die mittlere Gewichtszunahme für eine Behandlungsdauer von zwei bis drei Monaten beträgt dabei (Benkert & Hippius 2017):
- < 0,5 kg: Aripiprazol, Ziprasidon ,Lurasidon
- 0,5 – 1,5 kg: Amisulprid, Asenapin, Fluphenazin, Haloperidol
- 1,5 – 3 kg: Paliperidonb, Quetiapin, Risperidon, Sertindol
- > 3 kg: Clozapin, Olanzapin, Zotepin, Thioridazin
Hinsichtlich einer ungewollten Gewichtszunahme besonders riskante Wirkstoffe sind Clozapin und Olanzapin; hier sind 10 – 40 % der Patienten von einer Gewichtszunahme > 10 % des Ausgangsgewichts betroffen, wobei sich nach ca. einem Jahr unter Therapie meist eine Plateauphase einstellt (Benkert & Hippius 2017).
Komplexe Ursachen der Gewichtszunahme
Die komplexen pathophysiologischen Zusammenhänge sind nach wie vor nicht vollständig geklärt. Gerade bei sehr starken Gewichtszunahmen ist die Relevanz einer genetischen Disposition (MC4R-Gen) wahrscheinlich. Auf die verschiedenen Erklärungsansätze und Hypothesen soll hier nicht en detail eingegangen werden; entsprechende Erläuterungen finden sich in der speziellen Fachliteratur Benkert & Hippius 2017, Zeiss et al. 2017).
Allein für den Zusammenhang von Antidepressiva und Körpergewichtsveränderungen werden ätiologische Faktoren wie eine Sympathikus-Aktivierung, eine gesteigerte Synthese von Entzündungsmediatoren und Veränderungen der Hypothalamus-Hypophysen-Nebennierenrinden-Achse (HPA-Achse) mit jeweils komplexen Sekundäreffekten diskutiert (Joseph & Golden 2016, Champaneri et al. 2010). Bei einzelnen Substanzen (z. B. Bupropion) ist die Einnahme nicht mit einer Gewichtszunahme, sondern mit Appetitminderung und Gewichtsabnahme assoziiert (Lee et al. 2016).
Bei den Antipsychotika dagegen stehen die Modulation diverser Neurotransmittersysteme mit Aktivierung des Appetitzentrums sowie hormonelle Wirkungen als Ursache von Körpergewichtsveränderungen unter der Therapie im Vordergrund (Roerig et al. 2011). Auch der negative Einfluss der meisten Antipsychotika auf den Energieumsatz scheint hier eine Rolle spielen (Stefanidis et al. 2009).
Blockade von Histamin-Rezeptoren als mögliche Hauptursache
Wesentlichen Anteil an der Gewichtszunahme bei Antipsychotika scheinen hemmende Partialwirkungen am Histaminrezeptor H1 zu besitzen (Kroeze et al. 2003). So korreliert die Gewichtszunahme nach Therapiebeginn sowohl bei Antipsychotika als auch bei Antidepressiva mit der H1-Rezeptoraffinität des jeweiligen Wirkstoffs: je höher die H1-blockierende Partialwirkung, desto stärker die Gewichtszunahme (Serretti & Mandelli 2010). Bei den als Antiallergika eingesetzten Antihistaminika ist dieser Zusammenhang bereits länger bekannt.
Kann man die Gewichtszunahme vorhersehen?
Immer wieder wird diskutiert, ob es prädiktive Faktoren gibt, die der (mehr oder weniger) sicheren Vorhersage dienen, bei welchen Patienten die unerwünschten metabolischen Effekte auftreten werden und bei welchen nicht. Bislang sind keine wirklich aussagekräftigen prädiktiven Faktoren dieser Art bekannt, sodass man im klinischen Alltag nicht weiß, welcher Patient für diese Nebenwirkungen besonders prädestiniert ist. Verschiedene Studien liefern jedoch einzelne Hinweise:
So deutet bei Antidepressiva eine frühe Gewichtszunahme zu Therapiebeginn auf eine später fortgesetzte Gewichtszunahme hin, während Patienten, die die ersten Therapiewochen ohne Gewichtszunahme hinter sich bringen, auch perspektivisch ein geringeres Risiko für eine Gewichtszunahmen besitzen. Weitere Faktoren, die eine spätere Gewichtszunahme begünstigen, sind ein eher niedriger/normaler BMI zu Therapiebeginn, eine schwere Depression und das Vorhandensein psychotischer Symptome neben der Depression (Kloiber et al. 2015).
Risikofaktoren für die Gewichtszunahme im Laufe der Therapie sind bei Antipsychotika (Neuroleptika) ein niedriger Ausgangs-BMI (Gebhardt et al. 2009), Begleit-Medikation mit Antidepressiva, sog. Negativsymptomatik (Affekt- und Antriebsreduktion) sowie Behandlung der ersten psychotischen Episode (first episode psychosis) (Strassnig et al. 2007). Bei Olanzapin ist eine Gewichtszunahme innerhalb der ersten Wochen prädiktiv für die weitere Gewichtszunahme.
Insgesamt sind die metabolischen Effekte der Antipsychotika vermutlich weniger von der Dosis, als vielmehr von der Therapiedauer abhängig (Bak et al. 2014). Mehr als die Hälfte der Patienten, die Antipsychotika langfristig einnehmen, zeigen einen BMI > 30 kg/m².
Störung des Zuckerstoffwechsels relevant
Prädisponierend für die Entwicklung einer pathologischen Glucosetoleranz sind insbesondere Olanzapin, Quetiapin und Perazin (Tabelle 2); erhöhte Blutzuckerkonzentrationen und assoziierte Störungen können hier auch ohne vorhergehende Gewichtszunahme auftreten. Für Clozapin gibt es Berichte über die Erstmanifestation eines Diabetes mit tödlich verlaufender Ketoazidose. In diesen Konstellationen besitzt daher die regelmäßige Kontrolle von Blutzuckerspiegel und HbA1c-Werten eine besondere Bedeutung (Tabelle 3).
Wirkstoffspezifische Nebenwirkungen auf den Stoffwechsel
Zugunsten von Übersichtlichkeit und Anwendbarkeit in der Praxis wird an dieser Stelle auf die detaillierte Diskussion der Studienlage zu allen gängigen Wirkstoffen verzichtet. Stattdessen liefern Tabelle 1 (Antidepressiva) und Tabelle 2 (Antipsychotika) einen schnellen Überblick. Beiden Tabellen können auf verschiedene Weisen praktisch genutzt werden:
- Identifizierung der pharmakotherapeutischen Ursache eines aufgetretenen Effekts (z. B. Gewichtszunahme) (Beispiel: Treten bei einem Patienten erstmals Hyperglyklämien auf, kann die Medikationsliste auf typischerweise auslösende Antipsychotika wie Perazin, Quetiapin oder Olanzapin geprüft werden.)
- ernährungstherapeutische und diagnostische Antizipation häufiger/typischer metabolischer Effekte eines bestimmten Wirkstoffs (Beispiel: diätetische Antizipation der Gewichtszunahme bei Therapiebeginn mit Clomipramin bereits vor Gewichtszunahme)
- Auswahl eines Wirkstoffs unter Berücksichtigung des individuellen Risikoprofils des Patienten (Beispiel: Bei Patienten mit bestehender Fettstoffwechselstörung sollte Paroxetin zurückhaltender eingesetzt werden als bei anderen Patienten.)


Wichtig für die Praxis: regelmäßiges Monitoring durchführen
Bei Patienten unter Psychopharmaka-Therapie sollten regelmäßig anthropometrische und laborchemische Daten erfasst werden, um metabolische Nebenwirkungen rechtzeitig erkennen und ggf. gegensteuern zu können; Tabelle 3 zeigt diese Monitoring-Empfehlungen für Patienten unter Therapie mit Antipsychotika. Bei Anwendung von Antidepressiva sollte die regelmäßige Gewichtskontrolle bei Mirtazapin, Lithium und den meisten trizyklischen Antidepressiva (z. B. Amitriptylin, Doxepin, Trimipramin, Imipramin usw.) durchgeführt werden.
Anhaltspunkte einer signifikanten Gewichtszunahme ist eine Steigerung um > 7 % des Körpergewichts in den ersten 3 – 12 Monaten der Therapie.
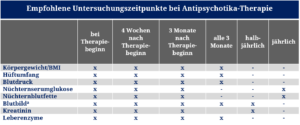
Möglichkeiten zur Reduktion metabolischer Nebenwirkungen
Kommt ein Wirkstoffwechsel zu einem Arzneistoff mit günstigerem Risikoprofil aufgrund der spezifischen Indikation und Nutzen-Risiko-Abwägung nicht infrage, können metabolische Nebenwirkungen häufig durch geeignete Arzneimittel kontrolliert bzw. abgemildert werden. Die meisten Daten zur Gewichtsreduktion bei Patienten unter antipsychotischer Medikation existieren für Orlistat (Fiedorowicz et al. 2012, Tchoukhine et al. 2011) und Metformin (off-label-Anwendung bei Gewichtszunahmen unter Clozapin und Olanzapin) (Wang et al. 2012, Jarskog et al. 2013).
Antipsychotika mit geringem Risiko für eine Gewichtszunahme sind v. a. Aripiprazol, Lurasidon, Paliperiodon (in niedriger Dosierung) und Ziprasidon (Benkert & Hippius 2017).
Als nicht-medikamentöse Optionen zur Kontrolle metabolischer Nebenwirkungen kommen verhaltenstherapeutische und diätetische Maßnahmen infrage. Trotz einzelner Studien zur Effektivität diätetischer Interventionen gibt es dazu keine aussagekräftigen systematischen Untersuchungen (Green et al. 2015a, Green et al. 2015b, Daumit et al. 2013). Hier besteht also definitiv weiterer Forschungsbedarf. Bis dahin kann über die Wirksamkeit entsprechender Maßnahmen (Einzelschulungen, Gruppenschulungen, Art der Intervention) nur spekuliert werden. Besondere Bedeutung besitzt folglich die Prävention in Form der gezielten Auswahl des Arzneistoffs und antizipierender Ernährungsinterventionen und Lebensstil-Modifikationen.
Vor diesem Hintergrund sollten Ernährungsfachkräfte die wirkstoffspezifischen Zusammenhänge zwischen Antidepressiva, Antipsychotika und metabolischen Veränderungen gut kennen. Damit besteht die Möglichkeit, im Einzelfall erwartbare Nebenwirkungen durch diätetische Maßnahmen abzumildern oder zu verhindern.
Umgekehrt erlaubt dieses Wissen die Zuordnung metabolischer Veränderungen zu einzelnen Arzneistoffen; durch diese Identifizierung eines Auslösers kann die Möglichkeit des Wirkstoffwechsels zur Diskussion gestellt werden. Und nicht zuletzt kann die Kenntnis der empfohlenen Kontrolluntersuchungen bei Patienten mit Antipsychotika-Therapie dazu beitragen, dass auch Ernährungsfachkräfte zur Wahrnehmung dieser Untersuchungen anhalten und motivieren können.
Das Wichtigste zu den metabolischen Nebenwirkungen von Psychopharmaka:
- Metabolische Effekte von Psychopharmaka sind sehr häufig; dies gilt insbesondere für appetitsteigernde Wirkungen und die Zunahme von Körpergewicht.
- Besonders stark mit einer Gewichtszunahme assoziiert sind Antipsychotika (Neuroleptika) und einige Antidepressiva (Mirtazapin, Lithium, Trizyklika).
- Resultierende metabolische Veränderungen sind pathophysiologisch relevant, da sie sich negativ auf die kardiovaskuläre Krankheitslast und Sterblichkeit der Patienten auswirken können.
- Insbesondere bei Patienten unter Therapie mit Antipsychotika sollte auf die regelmäßige Durchführung metabolischer Monitoring-Untersuchungen geachtet werden.
- Wirkstoffspezifische metabolische Nebenwirkungen (v. a. Gewichtszunahme) können antizipiert und durch geeignete Ernährungsinterventionen abgemildert oder verhindert werden. Alternativ sollte ärztlicherseits auch ein Wirkstoffwechsel erwogen werden, falls die Nebenwirkungen die Lebensqualität des Patienten relevant beeinträchtigen. Zusätzlich kann die Gewichtskontrolle auch durch Gabe von Orlistat bzw. Metformin (off-label) verbessert werden.
Hier gibt’s den Vortrag zu metabolischen Nebenwirkungen von Psychopharmaka von der Ernährung2018 in Kassel.
- Ernaehrungsmedizin.blog jetzt auf Instagram! - 18. Dezember 2023
- Neue Studie: Adipositas als Risikofaktor für Darmkrebs stark unterschätzt - 9. Juni 2023
- Ernährungsstrategie der Bundesregierung: Gerecht, gesund und nachhaltig soll sie sein - 21. Dezember 2022

Bupropion ist kein Antipsychotikum. Eher das gegteil: Ein Amphetamin-Derivat.
Vielen Dank für diesen Hinweis, der natürlich richtig ist. Die entsprechende Textstelle wurde korrigiert.
Wie kann den Patienten geholfen werden, die auch nach dem Absetzen der Antidepressiva unter Stoffwechselstörung leiden?
Das kann pauschaul leider nicht beantwortet werden. Dazu sollten Sie Kontakt mit Ihrer Hausärztin/Ihrem Hausarzt aufnehmen.
Ich hatte lange Olanzapin und kann die Nebenwirkungen mit deutlicher Gewichtszunahme bestätigen.
Aktuell wurde umgestellt, ich versuche nun mit low carb etwas Gewicht zu verlieren, hoffe sehr das es klappt..
Danke für den informativen Beitrag.